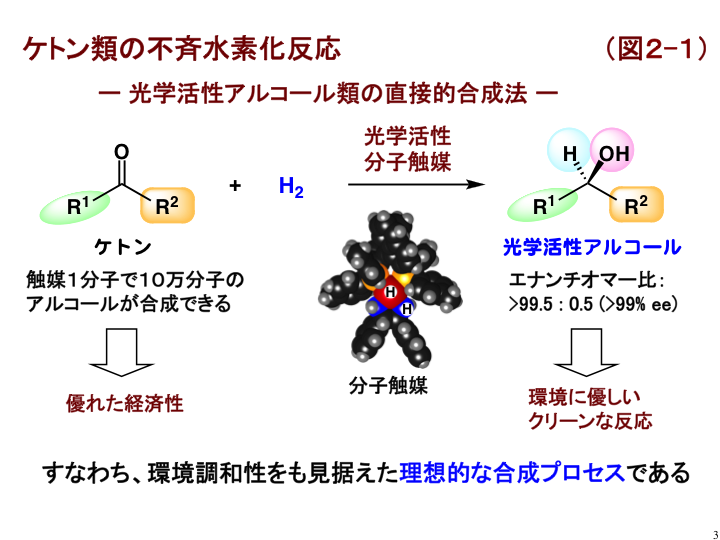
わたしたちは、医薬や香料などの原料として需要が非常に多い「光学活性アルコール類」の作り分けに着目して研究を進めてきました。光学活性とは、ある分子群が右手型あるいは左手型のどちらか一方だけである状態を示します。アルコールの合成にはいろいろな合成法が考えられますが、わたしたちが選んだのは、「ケトン類の不斉水素化反応」です。図2-1にその概要を示します。ケトンとよばれる平面性分子の表または裏から選択的に水素を付加させることで、光学活性アルコールを作り分ける、すなわち、立体選択的(この場合はエナンチオ選択的)に合成することができます。ただし、安定な分子であるケトンと水素をただ混ぜただけでは反応しません。そこで、わたしたちは、ケトンの水素化を効率的にサポートする光学活性な「分子触媒」を使うことにしました。優れた分子触媒は活性が高く、触媒1分子で10万分子ものアルコールを合成でき、経済性にとても優れています[B1]。これまでにわたしたちは、触媒1分子で240万分子もの光学活性アルコールを作り出すことのできる触媒も開発しており、キログラム単位で目的物を得ることにも成功しています [B2]。また、この反応はケトンに水素を付加させるだけで、副生成物を出すことなく光学活性アルコールを非常に高い立体選択性で与え、環境にも優しい反応です。(右手型と左手型分子のモル比が>99.5 : 0.5のとき、>99% eeと表します。)したがって、ケトン類の不斉水素化は、環境調和をも見据えた理想的な合成プロセスとなり得るのです。
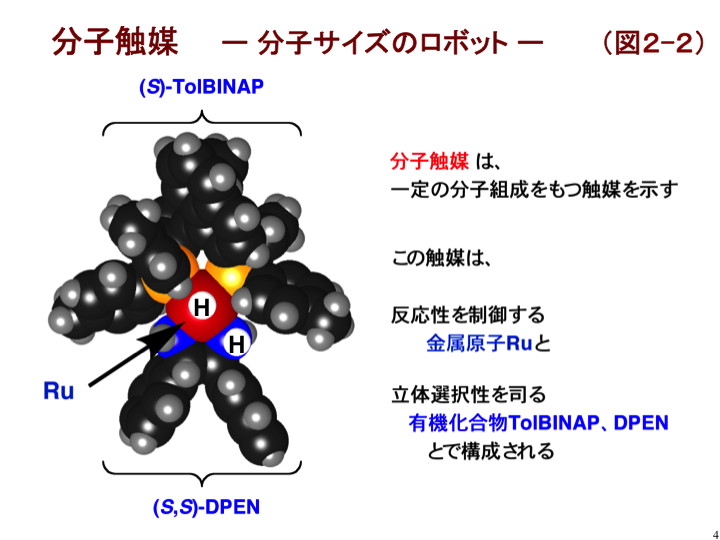
わたしたちの用いている分子触媒の一例を、図2-2に示します。この触媒は、一定の分子組成を持ち、反応性を制御する金属原子ルテニウムと立体選択性を司る光学活性な有機化合物(配位子とよびます)から構成されています。このように、金属原子と配位子から形作られる分子のことを「金属錯体」と呼びます。この金属錯体が不斉水素化反応において精緻な機能を示す分子触媒となるのです。まさに「分子サイズのロボット」です。どれだけ優れた触媒を産み出せるかが、わたしたち研究者の腕の見せ所となります。
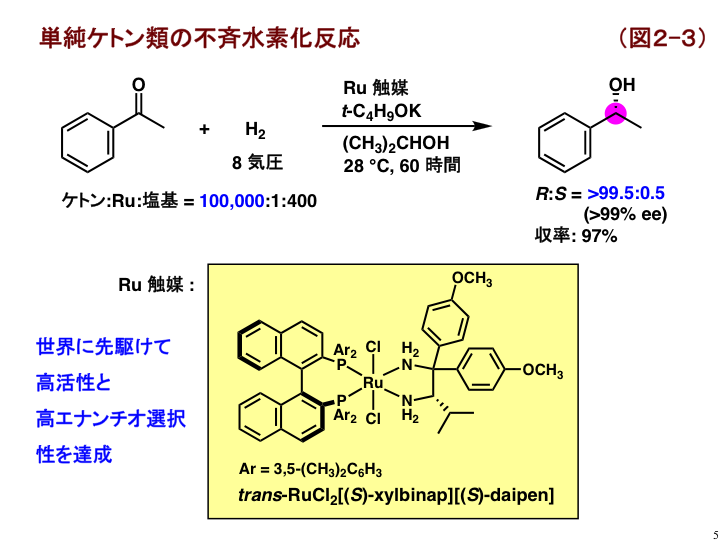
このような分子触媒を種々開発することで、単純な構造をもつケトン類の不斉水素化反応に世界で初めて成功しました[B1]。例えば、図2-3に示すように、XylBINAPとDAIPENとよばれる光学活性配位子をもつルテニウム錯体を用いると、10万倍量のケトンを水素化し、対応する(R)体(右手型)のアルコールを立体選択的に合成することができます[B3]。
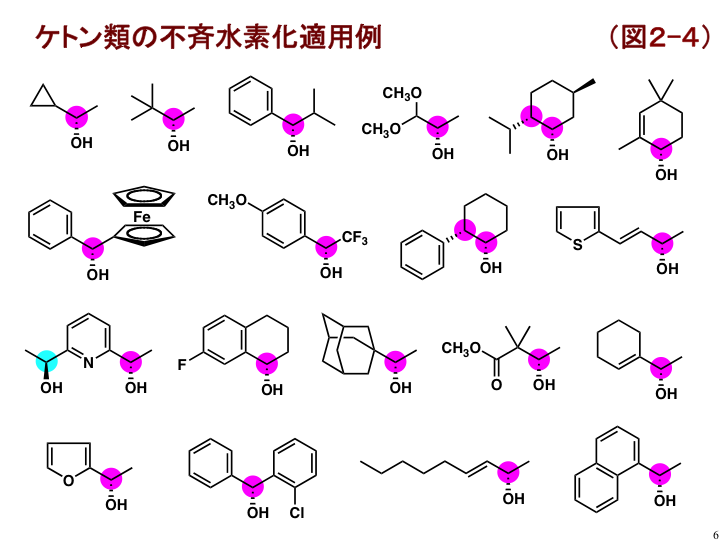
この触媒は、広範囲のケトン類の不斉水素化反応に対して適用することができます。図2-4に合成できる光学活性のアルコール例を示します[B1,B3]。化学系企業との共同研究により、触媒の試薬販売や光学活性アルコールの受託合成を開始することができました。(PDF)
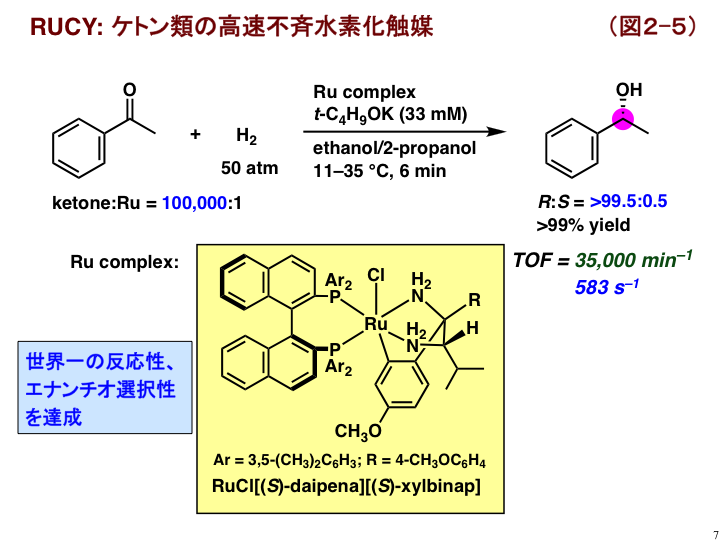
分子触媒の設計では、金属と配位子の組み合わせや錯体の構造が極めて重要になります。わたしたちは適切な分子設計を施すことで、極めて高い水素化活性を示す分子触媒を開発することに成功しました。図2-5に示すようにRUCYと名付けられたこの触媒は、先ほど示した触媒とは異なり、特異なルテナビシクロ骨格をもち、適切な条件下で10万倍量のアセトフェノン(ケトン)を僅か6分ですべてアルコールに変換できます[B4]。その仕事効率は毎分3万5千回、毎秒では583回で、F1マシンのエンジンの回転速度を優に凌駕します。エナンチオ選択性もほぼ完璧で、革新的な進歩であると考えています。この触媒も社会に役立てるため試薬販売を開始しました。
ひとくちにケトンといっても様々な構造があり、一つの触媒でそのすべてを不斉水素化することはできません。そこでわたしたちは、特異な構造をもつケトンにも対応できるテーラーメイドな触媒開発に挑戦しました。その成果の一例を図2-6に示します。カルコンのアリルアルコールへの水素化では、TolBINAPとDMAPENを配位子に用いることで、酵素法を含め、初めて高立体選択的な還元を達成しました[B5]。(PDF)
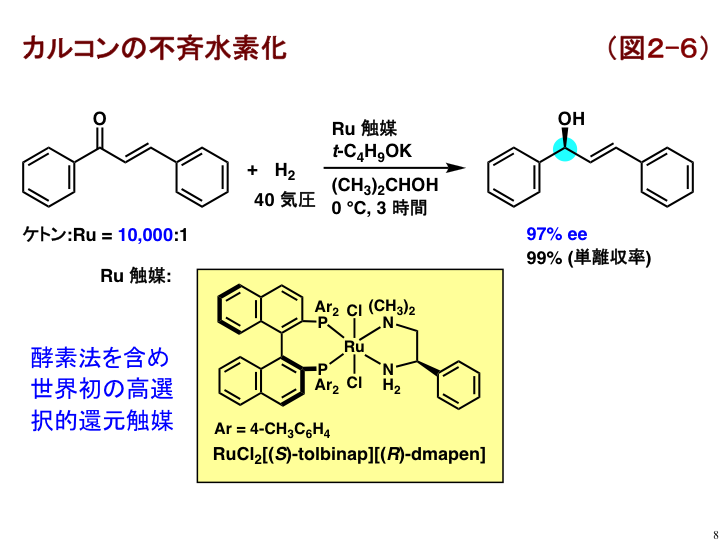
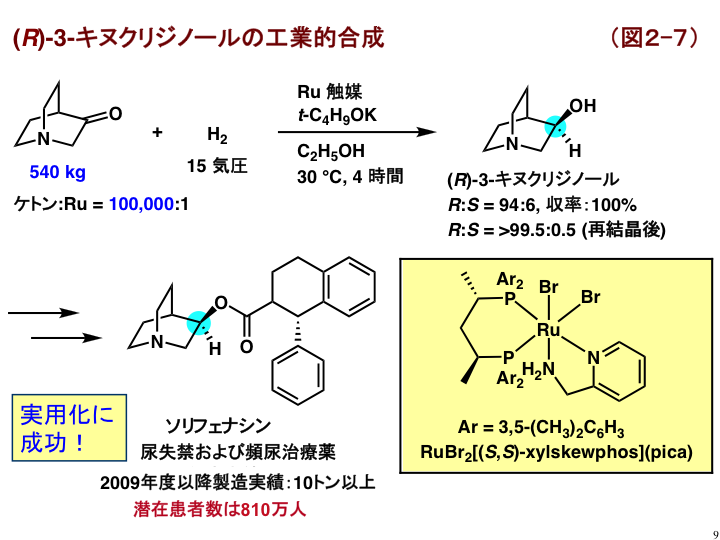
図2-7に示すように、XylSkewphosとα-ピコリルアミン(PICA)を配位子とするルテニウム錯体は極めて高い触媒活性を示し、混み合ったビシクロ[2.2.2]骨格をもつ3-キヌクリジノンを効率的に3-キヌクリジノールに水素化することができます[B6]。10万倍量のケトンを4時間以内に還元できます。化学系企業との共同研究で、540キロ規模の反応も達成し、実用化に成功しました。生成物である光学活性3-キヌクリジノールは尿失禁および頻尿などの治療薬として知られるソリフェナシンの鍵となる合成原料です。2009年度以降で10トン以上製造しています。(PDF)
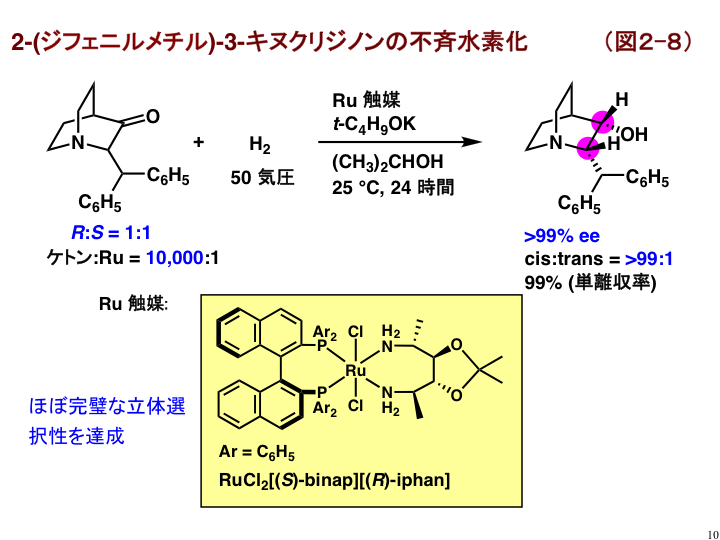
さらに複雑な構造をもつ2-(ジフェニルメチル)-3-キヌクリジノンの水素化には、図2-8に示すBINAPとIPHANを配位子とする錯体が非常に優れていることがわかりました[B7]。4種類可能性がある生成物のうち、1種類だけがほぼ完璧な立体選択性で得られます。
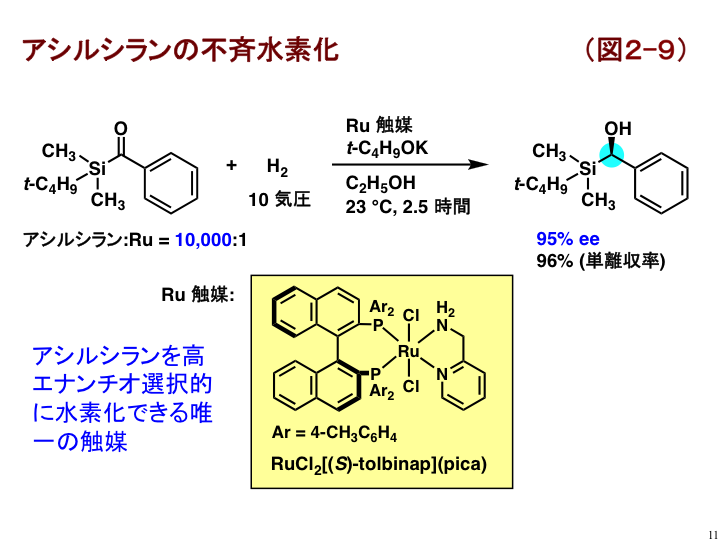
ケトンのケイ素等価体として注目されているアシルシランは、反応点近傍が立体的にかさ高いことに加えて、水素化条件に不安定であるため、有効な不斉水素化触媒が知られていませんでした。わたしたちは、図2-9に示すTolBINAPとPICAを配位子とする錯体を触媒に用いることで、世界に先駆けてアシルシラン類の高速かつ高立体選択的水素化の開発に成功しました[B8]。
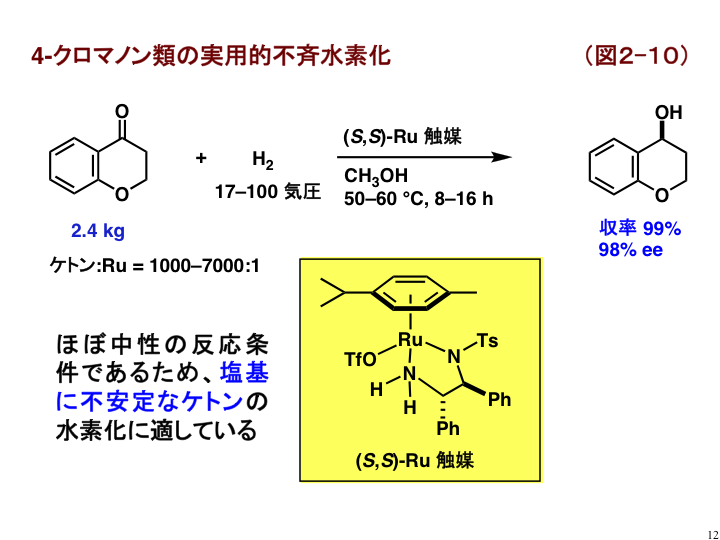
ここまで示してきた触媒は塩基による活性化を必要とするため、塩基性条件で不安定なケトン類の不斉水素化を行うのは困難でした。わたしたちは図2-10に示したアレーン/ルテニウム型の触媒が、メタノール中で容易にトリフラートアニオン(CF3SO3–)を乖離し、塩基無添加のほぼ中性条件で水素化活性を示すことを見いだしました[B9]。例えば塩基で分解し易い4-クロマノン(ケトン)を定量的に水素化することができます。エナンチオ選択性も高く、キログラムスケールの反応に適応できるため、化学系企業で実用化検討が行われています。また、すでに触媒は市販されています。(PDF)
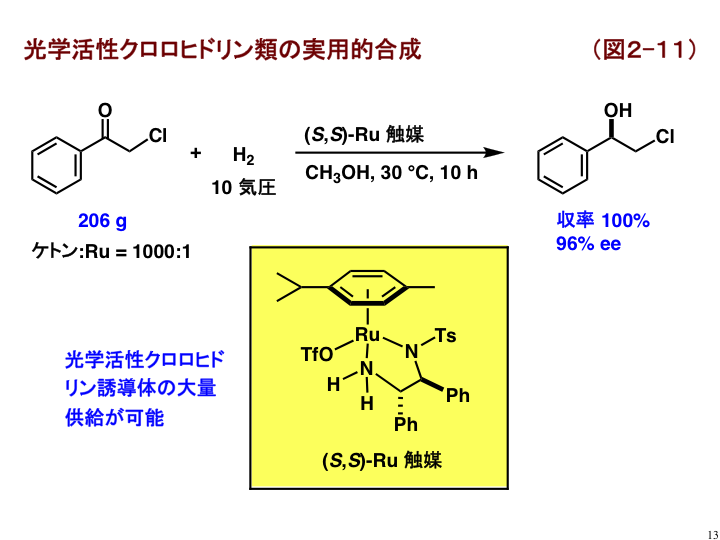
α-クロロケトン類も塩基性条件で分解し易く、不斉水素化が困難な基質でしたが、光学活性アレーン/ルテニウム触媒を用いることで問題を解決することができました(図2-11)[B10]。世界初の成功例です。200グラム規模の反応も容易に行えます。
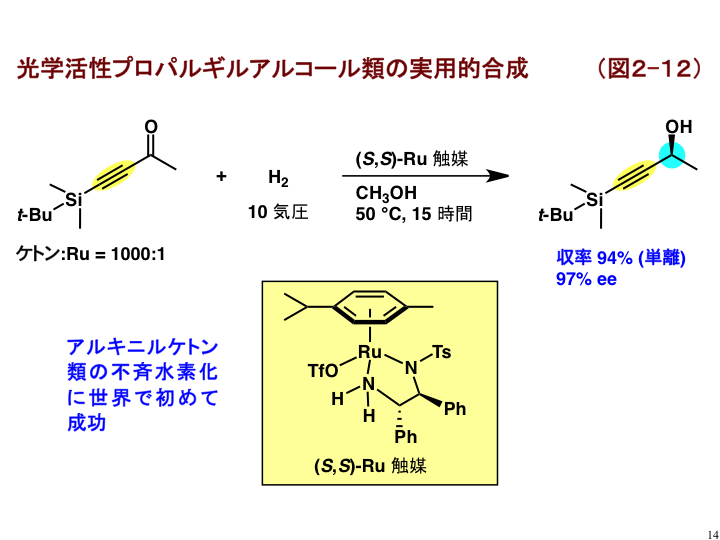
光学活性アレーン/ルテニウム触媒は、塩基に極めて不安定なアルキニルケトン類の不斉水素化にも有効で、生理活性物質合成で頻繁に用いられる光学活性プロパルギルアルコールを高収率、高エナンチオ選択的に与えます(図2-12)[B11]。一般にもっとも水素化され易いアルキニル基が、まったく還元されなかったことは特筆に値します。世界初の成功例であり、実用的展開が期待されます。
α-ヒドロキシケトン類も塩基に不安定で、その効率的な不斉水素化法の開発が求められていましたが、図2-13に示す光学活性Cp*イリジウム触媒を用いることで、目的を達成しました[B12]。このケトンは電子的にα-クロロケトン類に似た性質をもっていると思われますが、Cp*イリジウム触媒と等電子的なアレーン/ルテニウム触媒では反応性、選択性ともに満足な結果は得られませんでした。また、配位子窒素上の置換基も触媒性能に影響を与え、メシル基(Ms基:CH3SO3)が最適であることがわかりました。
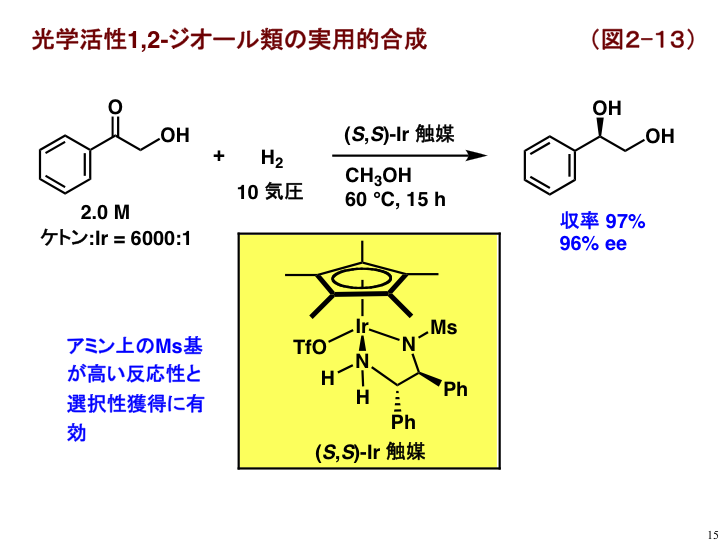
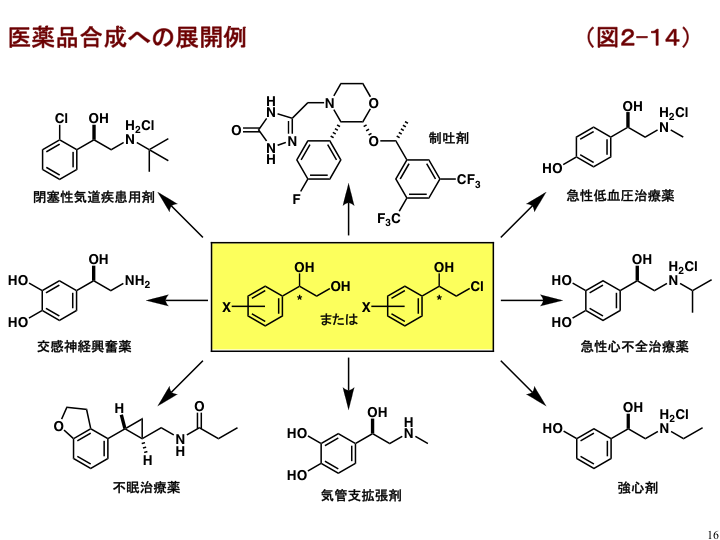
図2-14に示すように、光学活性クロロヒドリン類や1,2-ジオール類は多様な医薬の中間体として用いられています。わたしたちの不斉水素化反応が、有用物質供給に貢献できるよう検討を続けています。