カルバモイル化によるラセミ体ヒドロキシラクトン類・エステル類の速度論分割
光学活性ルイス酸触媒を用いる反応の多くは、高い立体選択性を示しますが、多くの触媒量を必要とします。わたしたちは、この主な原因を1)ルイス酸触媒自体の不安定性と、2)生成物が触媒を失活してしまう「生成物阻害」によるものであると考えました。そこで、図6-1に示すように、水などの共存に安定な遷移金属錯体を用い、生成物阻害が起こり難いと期待されるα-ヒドロキシラクトン類のカルバモイル化において高いルイス酸触媒活性の達成を目指しました。少し専門的な話になりますが、α-ヒドロキシラクトンは金属に配位して安定な五員環キレートを形成する一方で、生成物のカーバメートは安定性の低い七員環キレートとなるため、生成物阻害を避けられると考えたからです。
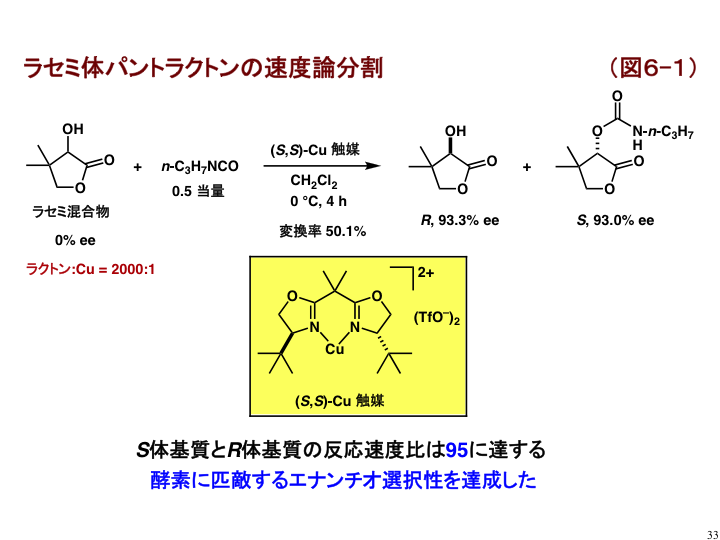
触媒として、光学活性なビス(オキサゾリン)配位子をもつ二価銅カチオン性錯体を用い、ラセミ体パントラクトンと0.5当量のエチルイソシアナートの反応を検討しました。2000分の1当量の触媒を用いると、0 °C、4時間で反応は完結し、未反応のRアルコールとSカーバメートがそれぞれ93.3% ee、93.0% eeで得られました[F1]。この結果は、(S)-パントラクトンがR体よりも95倍速く反応することを表し、光学活性銅触媒が酵素に匹敵する高い水準で分子の左右を識別できることを示します。また、ヒドロキシラクトンの構造を変えることにより、最高209倍の速度差が得られました。
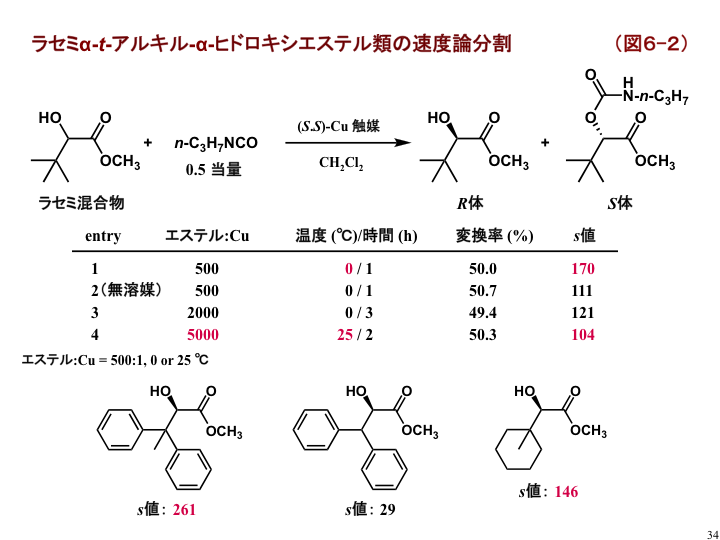
本不斉カルバモイル化を用いることで、他法では適用困難なα位に第三級アルキル基をもつα-ヒドロキシエステル類を効率的に速度論分割することができました。例えば、図6-2に示すラセミ混合物の反応では、500分の1当量の触媒を用いると0 ℃、1時間で50%の変換率に達し、s値は極めて高い170です[F2]。無溶媒でも高選択的に反応は進行します。触媒量を2000分の1当量にしても3時間で反応はほぼ終了し、5000分の1当量でも25 ℃であれば2時間で変換率50%に達し、s値が100を越えるような高い選択性が得られます。
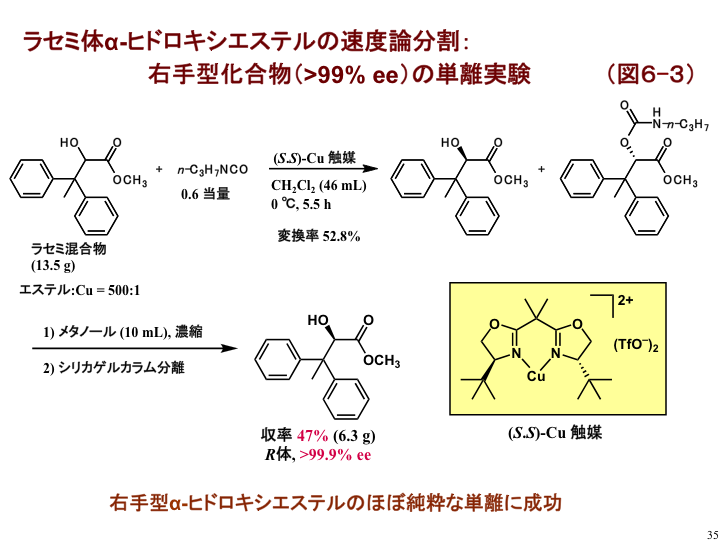
0.6当量のイソシアン酸エステルを用い、0 ℃で変換率約53%まで反応させることで、光学的にほぼ純粋なヒドロキシエステルを47%の単離収率で得ました(図6-3)[F2]。本反応の実用性の高さを示した結果です。
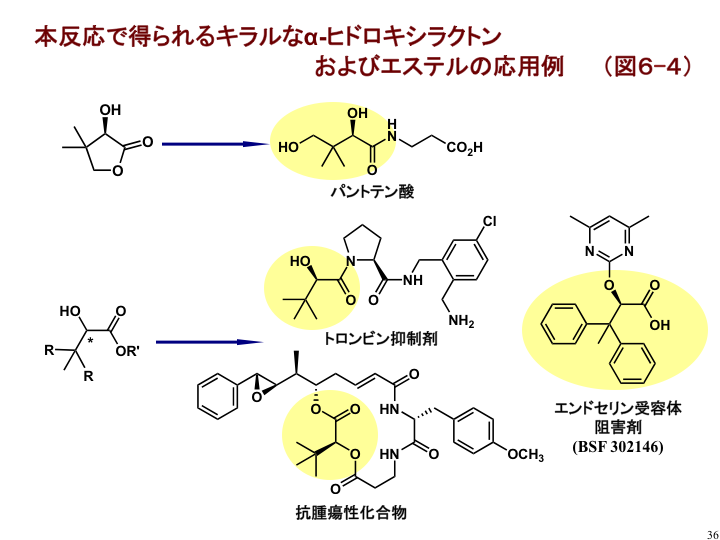
本反応の合成展開例を図6-4に示しました。その数は増加傾向にあり、本反応の特徴が活かせるものと期待しています。